- Exercice de conversion tiré du livre Chimie des solutions, 2e édition, Eddy Flamand, Modulo, 2003 :
 La stratégie consiste à remplir une table de conversion avant de répondre aux questions. Transcrivez d'abord dans la table sur la ligne "Masse" la donnée principale du problème, soit le pourcentage massique, saisissez par défaut la valeur 100,0 pour la masse de la solution et passez à la question suivante.
La stratégie consiste à remplir une table de conversion avant de répondre aux questions. Transcrivez d'abord dans la table sur la ligne "Masse" la donnée principale du problème, soit le pourcentage massique, saisissez par défaut la valeur 100,0 pour la masse de la solution et passez à la question suivante.
Solution = H2SO4 + Eau Masse ? g = + Nombre de mol = + Volume = + Solution = H2SO4 + Eau Masse 100,0 g = 96,0 g + 4,0 g Nombre de mol (Pas nécessaire) = 0,979 mol + 0,222 mol Volume 54,3 mL = (Pas nécessaire) + (Pas nécessaire) 
a) Concentration 18,0 mol/L b) Fraction molaire du soluté 0,815 c) Molalité 245 mol/kg d) mH2SO4 dans 100,0 mL solution ? g Solution = H2SO4 + Eau Masse 100,0 g = 96,0 g + 4,0 g Nombre de mol (Pas nécessaire) = 0,979 mol + 0,222 mol Volume 54,3 mL = (Pas nécessaire) + (Pas nécessaire) 
a) Concentration 18,0 mol/L b) Fraction molaire du soluté 0,815 c) Molalité 245 mol/kg d) mH2SO4 dans 100,0 mL solution 177 g e) Vsolution pour préparer 500,0 mL à 3,0 mol/L ? mL - En résumé, on remplit la table à partir d'une expression fournie dans le problème (dans ce cas le pourcentage massique) sans trop se soucier des questions. Il est possible que la ligne "Volume" ne soit d'aucune utilité selon l'exercice.
Solution = Soluté + Solvant Masse À calculer = À calculer + À calculer Nombre de mol (facultatif) = À calculer + À calculer Volume À calculer = Non calculé + Non calculé
(Comme c'est le cas pour bien des solutions concentrées, le soluté (H2SO4) est majoritaire car ces solutions servent à préparer des solutions plus diluées dans lesquelles l'eau (solvant) devient majoritaire lors de la dilution.)a) Concentration 18,0 mol/L b) Fraction molaire du soluté 0,815 c) Molalité 245 mol/kg d) mH2SO4 dans 100,0 mL solution 177 g e) vsolution pour préparer 500,0 mL à 3,0 mol/L 83 mL
Notons enfin que la masse volumique de la solution et la masse molaire du soluté permettent le passage d'une ligne à une autre comme le montre ce schéma :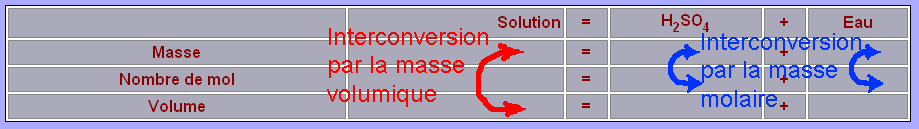
- Terminé



